Năm 1973, chiếc điện thoại di động đầu tiên trên thế giới ra đời trong phòng thí nghiệm của Motorola. Nó rất cồng kềnh, nhưng nhờ có pin niken-cadmium được tích hợp trong đó, nó có thể thực hiện các cuộc gọi di động theo thời gian thực mà không cần các mạch điện tử phức tạp.
Pin niken-cadmium là loại pin đầu tiên được tích hợp vào điện thoại di động và có kích thước tương đối cồng kềnh. Hầu hết các "Big Brother và Big Phone" phổ biến trong thế kỷ trước đều sử dụng pin niken-cadmium. Pin niken-cadmium có dung lượng thấp và chứa cadmium có độc tính cao, không có lợi cho việc bảo vệ môi trường sinh thái. Hơn nữa, pin niken-cadmium còn có tác dụng ghi nhớ rất rõ ràng: nếu chưa cạn kiệt nguồn điện trước khi sạc, dung lượng pin sẽ giảm dần theo thời gian.
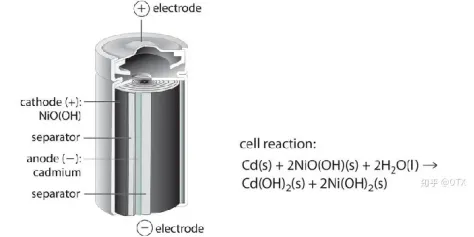 Cấu trúc cơ bản của pin niken-cadmium
Cấu trúc cơ bản của pin niken-cadmium
Năm 1990, Tập đoàn Sony của Nhật Bản lần đầu tiên phát triển pin hydrua kim loại niken. So với các thiết bị tiền nhiệm, pin hydrua kim loại niken không chỉ có thể được làm mỏng hơn và nhẹ hơn mà dung lượng của chúng cũng có thể được cải thiện một cách hiệu quả [3]. Sự xuất hiện của pin niken-hyđrua kim loại đã làm cho điện thoại di động trở nên di động hơn và có thể hỗ trợ các cuộc gọi dài hơn. Do đó, với sự xuất hiện của pin niken-hydrua kim loại, pin niken-cadmium cồng kềnh dần được thay thế và điện thoại di động nhỏ gọn trở nên phổ biến. Tuy nhiên, pin niken-kim loại hydrua vẫn có hiệu ứng bộ nhớ, đó là lý do tại sao thế hệ điện thoại di động trước đây cần phải xả hết điện trước khi sạc lại. Hơn nữa, do mật độ năng lượng hạn chế của pin niken-cadmium, điện thoại di động thời đó chỉ có thể hỗ trợ các tác vụ tương đối đơn giản như thực hiện cuộc gọi, vẫn còn kém xa so với hình thức điện thoại thông minh hiện tại của chúng ta.
Pin lithium sử dụng lithium kim loại làm điện cực âm lần đầu tiên được thương mại hóa. Năm 1970, Tập đoàn Panasonic của Nhật Bản đã phát minh ra pin lithium fluorocarbon, loại pin này có dung lượng lý thuyết lớn, công suất xả ổn định và khả năng tự phóng điện nhỏ. Tuy nhiên, loại pin này không thể sạc được và là loại pin lithium sơ cấp.
Vào những năm 1970, M. Stanley Whittingham, một nhà nghiên cứu của ExxonMobil, đã đề xuất nguyên lý sạc và xả pin của sự xen kẽ ion và công bố titan disulfide vào năm 1975. Bằng sáng chế về pin lithium. Năm 1977, nhóm Whittingham làm việc tại Exxon đã phát triển loại pin thứ cấp sử dụng hợp kim nhôm-lithium Li-Al làm điện cực âm và titan disulfide TiS₂ làm điện cực dương. Hợp kim nhôm-lithium có thể cải thiện độ ổn định của lithium kim loại. an toàn. Trong quá trình phóng điện, quá trình điện hóa xảy ra ở ắc quy là:
Điện cực âm: Li - e- → Li+
Điện cực dương: xLi+ + TiS₂+ xe- → LixTiS₂
Trong số đó, TiS₂ là một hợp chất phân lớp và tương tác giữa các lớp là Lực Van der Waals (Lực Van der Waals). Các ion lithium nhỏ hơn có thể đi vào các lớp TiS₂ và trải qua quá trình truyền điện tích cũng như lưu trữ các ion lithium, tương tự như Khi ép mứt vào bánh sandwich, quá trình này là sự xen kẽ của các ion [4] [5]. Trong quá trình phóng điện, các ion Li+ trong chất điện phân được chèn vào giữa các lớp TiS₂ của điện cực dương, nhận điện tích và hình thành LixTiS₂.
Pin lithium thứ cấp ở giai đoạn này chủ yếu sử dụng lithium kim loại làm vật liệu điện cực âm, tuổi thọ và độ an toàn của pin được cải thiện bằng cách cải tiến vật liệu điện cực dương. Là loại pin lithium thứ cấp được thương mại hóa sớm nhất, lithium kim loại được sử dụng làm vật liệu điện cực âm có điện thế âm thấp. Pin có mật độ năng lượng cao và tương đối di động. Tuy nhiên, độ an toàn của nó cũng bị nghi ngờ rộng rãi. Vào cuối mùa xuân năm 1989, pin lithium kim loại thế hệ đầu tiên do công ty Moli Energy của Canada sản xuất phát nổ, điều này cũng khiến việc thương mại hóa pin lithium kim loại rơi vào bế tắc.
Để nâng cao tính an toàn của pin lithium, việc phát triển vật liệu điện cực mới là rất quan trọng đối với pin lithium. Tuy nhiên, việc sử dụng các hợp chất lithium khác làm điện cực âm thay vì lithium sẽ làm tăng thế điện cực âm, giảm mật độ năng lượng của pin lithium và giảm dung lượng pin. Vì vậy, việc tìm kiếm vật liệu điện cực mới phù hợp cũng trở thành bài toán khó trong lĩnh vực nghiên cứu pin lithium.
Khoảng năm 1980, John Bannister Goodenough và những người khác giảng dạy tại Đại học Oxford ở Vương quốc Anh đã phát hiện ra lithium coban oxit LiCoO₂ (LCO), một hợp chất có thể chứa các ion lithium. LiCoO₂ có tiềm năng cao hơn các vật liệu catốt khác vào thời điểm đó. Điều này cho phép pin lithium sử dụng LiCoO₂ làm điện cực dương để cung cấp điện áp cao hơn và dung lượng pin cao hơn.
Tinh thể oxit lithium coban có cấu trúc phân lớp và thuộc hệ tinh thể lục giác . Trong số đó, mạng bát diện gồm các nguyên tử O và Co được sắp xếp trên mặt phẳng thành các lớp CoO₂ và các lớp CoO₂ được ngăn cách với nhau bằng các ion lithium và tạo thành kênh truyền ion lithium phẳng. Điều này cho phép oxit lithium coban vận chuyển các ion lithium nhanh hơn thông qua kênh ion lithium phẳng. Quá trình tách và chèn các ion lithium trong oxit lithium coban tương tự như quá trình xen kẽ. Oxit lithium coban có thể duy trì sự ổn định của cấu trúc tinh thể của nó trong quá trình tích điện và phóng điện nhẹ. Tuy nhiên, với việc loại bỏ dần các ion lithium, oxit lithium coban có xu hướng biến đổi thành hệ tinh thể đơn tà [2]. Trong pin lithium sử dụng lithium coban oxit làm điện cực dương, trong quá trình phóng điện, phản ứng xảy ra ở điện cực dương là:
Điện cực dương: Li1-xCoO₂ + xLi+ + xe- → LiCoO₂
So với titan disulfua, vật liệu catốt lithium coban oxit có tiềm năng catốt cao hơn, đồng thời cấu trúc phân lớp của lithium coban oxit có thể vận chuyển các ion lithium nhanh hơn, khiến nó trở thành vật liệu catốt tuyệt vời cho pin lithium-ion.
Cùng năm đó, Rachid Yazami đã phát hiện ra hiện tượng xen kẽ ion tuần hoàn của các ion lithium trong than chì và xác minh tính khả thi của than chì làm cực âm cho pin lithium [10]. Than chì có cấu trúc dạng lớp và tương tự như TiS₂, các lớp trong than chì được kết nối bởi lực van der Waals yếu, cho phép các ion lithium nhỏ hơn đi vào các lớp than chì và gây ra sự truyền điện tích.
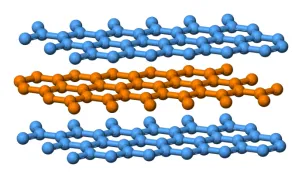 Than chì có cấu trúc phân lớp và các lớp được kết nối với nhau bằng lực van der Waals
Than chì có cấu trúc phân lớp và các lớp được kết nối với nhau bằng lực van der Waals
Trong bài báo năm 1983 của mình, Yazami đã sử dụng phương pháp điện phân trạng thái rắn polyethylene oxit-lithium perchlorate và sử dụng kim loại lithium làm điện cực âm và than chì làm điện cực dương để tạo thành pin sơ cấp. Trong quá trình phóng điện, than chì đóng vai trò là điện cực dương trải qua phản ứng sau:
nC + e- + Li+ → (nC, Li)
Khi đó xảy ra: (nC, Li) → LiCn
Trong quá trình phóng điện của pin ban đầu với than chì làm điện cực dương, các ion lithium trải qua phản ứng xen kẽ trong lớp than chì, xảy ra sự truyền điện tích và hợp chất LiCn được hình thành.
Tuy nhiên, pin lithium coban oxit vẫn còn nhiều vấn đề. Điện cực âm của pin, polyacetylene, có mật độ năng lượng thấp và độ ổn định thấp. Do đó, Akira Yoshino đã sử dụng vật liệu giống than chì mới “carbon mềm” thay vì polyacetylene làm vật liệu điện cực âm của pin, và chuẩn bị nguyên mẫu pin lithium-ion đầu tiên vào năm 1985 và xin cấp bằng sáng chế [10]. Nguyên mẫu pin lithium-ion do Akira Yoshino thiết kế đã trở thành nền tảng cho nhiều loại pin hiện đại.
So với pin lithium, pin nguyên bản do Akira Yoshino thiết kế sử dụng vật liệu cacbon làm điện cực âm và oxit lithium coban làm điện cực dương để loại bỏ lithium kim loại, vì vậy loại pin này còn được gọi là "pin lithium-ion" . Bởi vì trong pin lithium-ion lithium coban oxit, các ion lithium trải qua các phản ứng xen kẽ ở cả điện cực dương và âm, và sự truyền điện tích nhanh chóng đạt được thông qua sự xen kẽ nhanh chóng của các ion lithium, nên cấu trúc pin này còn được gọi một cách sống động là pin ghế bập bênh.
Năm 2019, Giải Nobel Hóa học đã được trao cho nhà khoa học người Mỹ John B. Goodenough, nhà khoa học người Anh M. Stanley Whittingham và nhà khoa học Nhật Bản Yoshino Akira Yoshino, để ghi nhận những đóng góp nghiên cứu của họ đối với pin lithium-ion.
 Người đoạt giải Nobel Hóa học 2023: từ trái sang phải, nhà khoa học Mỹ John B. Goodenough, nhà khoa học người Anh M. Stanley Whittingham và nhà khoa học Nhật Bản Akira Yoshino.
Người đoạt giải Nobel Hóa học 2023: từ trái sang phải, nhà khoa học Mỹ John B. Goodenough, nhà khoa học người Anh M. Stanley Whittingham và nhà khoa học Nhật Bản Akira Yoshino.
Sự xuất hiện của pin lithium-ion sử dụng vật liệu carbon làm điện cực âm và oxit lithium coban làm điện cực dương đã thúc đẩy sự phát triển của pin lithium-ion. Khi các nhà nghiên cứu dần dần nghiên cứu sâu hơn về pin lithium-ion, ba hệ thống đã được phát triển cho vật liệu cực âm của pin lithium-ion: lithium coban oxit (LCO), lithium sắt photphat (LFP) và mangan coban niken bậc ba (NMC/NCM). ) ). hệ thống. Trong số đó, hệ thống lithium coban oxit có dung lượng pin tương đối cao hơn và đóng vai trò quyết định trong lĩnh vực sản phẩm điện tử 3C như điện thoại di động và máy tính mà chúng ta thường sử dụng. Hệ thống lithium sắt photphat và hệ thống lithium bậc ba có độ ổn định cao hơn và được sử dụng rộng rãi trong các phương tiện năng lượng mới.
Sự xuất hiện của pin lithium-ion đã thay đổi hoàn toàn cách chúng ta sống. So với pin niken-cadmium và pin niken-hydrua kim loại, pin lithium-ion có mật độ năng lượng cao hơn, pin lithium-ion có cùng dung lượng pin sẽ dễ mang theo hơn và có thể hỗ trợ mức tiêu thụ điện năng cao cho điện thoại thông minh có nhiều chức năng phong phú. Đồng thời, hầu hết pin lithium-ion không có hiệu ứng nhớ và không cần phải xả hết trước khi sạc lại, do đó, pin lithium-ion có thể được sạc theo yêu cầu. So với pin lithium, tốc độ sạc của pin lithium-ion được cải thiện đáng kể. Và tốc độ sạc nhanh của pin lithium-ion hỗ trợ rất nhiều cho cuộc sống của chúng ta. Do đó, trong các tình huống ứng dụng như điện thoại di động, máy tính di động và phương tiện sử dụng năng lượng mới, pin lithium-ion đã dần thay thế pin niken-cadmium và pin hydrua kim loại niken trong một số tình huống nhờ hiệu suất tuyệt vời của chúng.
Đối với pin niken-cadmium, các hạt tinh thể cadmium ở điện cực âm của pin niken-cadmium được chuẩn bị thiêu kết tương đối thô, khi pin niken-cadmium không được sạc đầy và xả trong thời gian dài, các hạt tinh thể cadmium dễ bị đến sự tập hợp và kết tụ. Tại thời điểm này, nền xả thứ cấp được hình thành khi pin xả. Pin sẽ sử dụng nền xả thứ cấp này làm điểm cuối của quá trình xả pin, dung lượng pin sẽ thấp và pin sẽ chỉ ghi nhớ dung lượng thấp này trong quá trình xả tiếp theo. Đây là lý do tại sao điện thoại di động thế hệ cũ sử dụng pin niken-cadmium thường được khuyến nghị xả hết pin trước khi sạc. Tuy nhiên, với sự cải tiến liên tục của công nghệ xử lý pin niken-cadmium và pin hydrua kim loại niken, tác động của hiệu ứng bộ nhớ đến dung lượng pin liên tục giảm và tác hại của việc sạc đầy và xả đối với tuổi thọ pin dần trở nên rõ ràng.
 Pin niken-cadmium có hiệu ứng ghi nhớ đáng kể, trong khi pin lithium-ion hầu như không có hiệu ứng ghi nhớ. Và do mật độ năng lượng của pin lithium-ion cao hơn pin niken-cadmium nên pin lithium-ion chủ yếu được sử dụng trong điện thoại di động, máy tính và các sản phẩm khác của chúng ta. Vì vậy, khi sử dụng điện thoại thông minh hoặc máy tính sử dụng pin lithium-ion hàng ngày, chúng ta không cần lo lắng về hiệu ứng ghi nhớ của pin.
Pin niken-cadmium có hiệu ứng ghi nhớ đáng kể, trong khi pin lithium-ion hầu như không có hiệu ứng ghi nhớ. Và do mật độ năng lượng của pin lithium-ion cao hơn pin niken-cadmium nên pin lithium-ion chủ yếu được sử dụng trong điện thoại di động, máy tính và các sản phẩm khác của chúng ta. Vì vậy, khi sử dụng điện thoại thông minh hoặc máy tính sử dụng pin lithium-ion hàng ngày, chúng ta không cần lo lắng về hiệu ứng ghi nhớ của pin.
Sạc và xả pin lithium-ion quá mức dẫn đến giảm tuổi thọ
Lithium coban oxit có công suất lý thuyết cao, nhưng công suất thực tế của lithium coban oxit khác xa so với công suất lý thuyết trong quá trình sử dụng. Bởi vì sau khi chúng ta sạc và xả pin lithium-ion vượt quá dung lượng này, lithium coban oxit sẽ trải qua quá trình sạc và xả không thể đảo ngược mà chúng ta thường gọi là sạc quá mức hoặc xả quá mức cho pin. Quá trình này đi kèm với sự thay đổi pha cấu trúc của oxit lithium coban, làm giảm dung lượng của pin.
Khi pin bị sạc quá mức, một lượng lớn ion lithium được giải phóng khỏi điện cực âm của oxit lithium coban và các ion lithium còn lại không đủ để hỗ trợ cấu trúc ban đầu của oxit lithium coban, khiến tinh thể Li1-xCoO₂ thay đổi từ từ hệ tinh thể lục giác sang hệ đơn tà, cấu trúc lục giác ban đầu bị sụp đổ do thiếu sự hỗ trợ của ion. Trong quá trình này, sự biến đổi pha của oxit lithium coban không thể đảo ngược hoàn toàn, các thông số tế bào đơn vị của oxit lithium coban thay đổi, ứng suất thay đổi và các chỗ trống lithium ion bị nén, khiến dung lượng của pin lithium-ion bị suy giảm.
Tính không ổn định của pin lithium-ion điện áp cao
Ngoài sự thay đổi không thể đảo ngược về dung lượng pin do sự thay đổi pha cấu trúc của oxit lithium coban, việc tăng điện áp đầu ra của pin lithium-ion còn khiến các phản ứng phụ khác dễ xảy ra ở pin lithium-ion và tuổi thọ của lithium -ion pin bị giảm. Hiện nay, điện thoại thông minh trên thị trường thường sử dụng điện áp sạc và xả khoảng 4,4V. Điện áp cao có thể làm tăng dung lượng của pin lithium-ion và tăng tốc độ sạc và xả của pin lithium-ion. Nhưng điều tiếp theo là sự gia tăng các phản ứng phụ trên bề mặt điện cực của pin lithium-ion và một loạt tác dụng phụ như sự mất ổn định của chất điện phân ở điện áp cao.
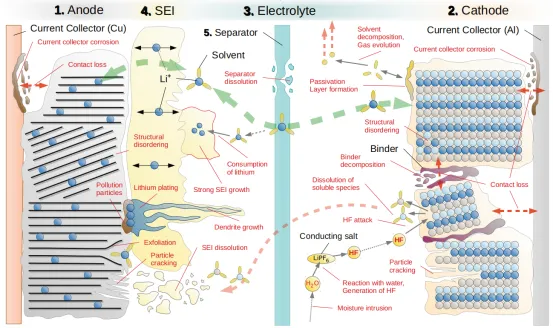 Cơ chế ảnh hưởng đến sự suy giảm tuổi thọ của pin lithium-ion điện áp cao
Cơ chế ảnh hưởng đến sự suy giảm tuổi thọ của pin lithium-ion điện áp cao
Chất điện phân của pin lithium-ion phản ứng ở giao diện rắn-lỏng với các điện cực dương và âm để tạo thành lớp thụ động bao phủ bề mặt điện cực. Lớp thụ động này có đặc tính của chất điện phân rắn, các ion Li có thể được đưa vào và tách ra một cách tự do thông qua lớp thụ động, do đó, màng thụ động này được gọi là “màng giao diện chất điện phân rắn” (gọi tắt là màng SEI). Quá trình hình thành màng SEI sẽ tiêu thụ một số ion lithium, gây ra tình trạng mất dung lượng pin lithium-ion không thể khắc phục được. Dưới tác động của điện áp cao, các phản ứng phụ trên bề mặt các điện cực này diễn ra nghiêm trọng khiến dung lượng pin giảm dần.
Không sạc điện thoại khi nó quá nóng hoặc quá lạnh. Khi điện thoại di động quá nóng, việc sạc pin lithium-ion trong điều kiện nhiệt độ cao cũng sẽ thay đổi cấu trúc điện cực dương và âm của pin lithium-ion, dẫn đến dung lượng pin bị suy giảm không thể khắc phục. Do đó, hãy cố gắng tránh sạc điện thoại trong điều kiện quá lạnh hoặc quá nóng, điều này cũng có thể kéo dài tuổi thọ sử dụng của điện thoại một cách hiệu quả.
 Thay pin kịp thời
Thay pin kịp thời
Trong quá trình sử dụng các sản phẩm kỹ thuật số như điện thoại di động, máy tính xách tay hoặc máy tính bảng, nếu phát hiện nắp lưng pin bị biến dạng, pin bị phồng hoặc các tình trạng bất thường khác thì chúng ta phải ngừng sử dụng kịp thời và thay pin cho nhà sản xuất, và cố gắng tránh các vấn đề do sử dụng pin gây ra.
Pin niken-cadmium là loại pin đầu tiên được tích hợp vào điện thoại di động và có kích thước tương đối cồng kềnh. Hầu hết các "Big Brother và Big Phone" phổ biến trong thế kỷ trước đều sử dụng pin niken-cadmium. Pin niken-cadmium có dung lượng thấp và chứa cadmium có độc tính cao, không có lợi cho việc bảo vệ môi trường sinh thái. Hơn nữa, pin niken-cadmium còn có tác dụng ghi nhớ rất rõ ràng: nếu chưa cạn kiệt nguồn điện trước khi sạc, dung lượng pin sẽ giảm dần theo thời gian.

Năm 1990, Tập đoàn Sony của Nhật Bản lần đầu tiên phát triển pin hydrua kim loại niken. So với các thiết bị tiền nhiệm, pin hydrua kim loại niken không chỉ có thể được làm mỏng hơn và nhẹ hơn mà dung lượng của chúng cũng có thể được cải thiện một cách hiệu quả [3]. Sự xuất hiện của pin niken-hyđrua kim loại đã làm cho điện thoại di động trở nên di động hơn và có thể hỗ trợ các cuộc gọi dài hơn. Do đó, với sự xuất hiện của pin niken-hydrua kim loại, pin niken-cadmium cồng kềnh dần được thay thế và điện thoại di động nhỏ gọn trở nên phổ biến. Tuy nhiên, pin niken-kim loại hydrua vẫn có hiệu ứng bộ nhớ, đó là lý do tại sao thế hệ điện thoại di động trước đây cần phải xả hết điện trước khi sạc lại. Hơn nữa, do mật độ năng lượng hạn chế của pin niken-cadmium, điện thoại di động thời đó chỉ có thể hỗ trợ các tác vụ tương đối đơn giản như thực hiện cuộc gọi, vẫn còn kém xa so với hình thức điện thoại thông minh hiện tại của chúng ta.
Sự trỗi dậy của pin lithium
Kim loại lithium được phát hiện vào thế kỷ 19. Lithium có những ưu điểm độc đáo như một loại pin chính do mật độ tương đối thấp, dung lượng cao và tiềm năng tương đối thấp. Tuy nhiên, lithium là một nguyên tố kim loại kiềm rất dễ phản ứng, dẫn đến yêu cầu môi trường rất cao đối với việc lưu trữ, sử dụng hoặc xử lý lithium kim loại và phức tạp hơn nhiều so với các kim loại khác. Vì vậy, trong quá trình nghiên cứu pin lithium sử dụng lithium làm vật liệu điện cực, các nhà khoa học đã khắc phục nhiều vấn đề nghiên cứu bằng cách liên tục phát triển và cải tiến pin lithium, sau nhiều công đoạn cuối cùng họ đã tạo ra được như ngày nay.Pin lithium sử dụng lithium kim loại làm điện cực âm lần đầu tiên được thương mại hóa. Năm 1970, Tập đoàn Panasonic của Nhật Bản đã phát minh ra pin lithium fluorocarbon, loại pin này có dung lượng lý thuyết lớn, công suất xả ổn định và khả năng tự phóng điện nhỏ. Tuy nhiên, loại pin này không thể sạc được và là loại pin lithium sơ cấp.
Vào những năm 1970, M. Stanley Whittingham, một nhà nghiên cứu của ExxonMobil, đã đề xuất nguyên lý sạc và xả pin của sự xen kẽ ion và công bố titan disulfide vào năm 1975. Bằng sáng chế về pin lithium. Năm 1977, nhóm Whittingham làm việc tại Exxon đã phát triển loại pin thứ cấp sử dụng hợp kim nhôm-lithium Li-Al làm điện cực âm và titan disulfide TiS₂ làm điện cực dương. Hợp kim nhôm-lithium có thể cải thiện độ ổn định của lithium kim loại. an toàn. Trong quá trình phóng điện, quá trình điện hóa xảy ra ở ắc quy là:
Điện cực âm: Li - e- → Li+
Điện cực dương: xLi+ + TiS₂+ xe- → LixTiS₂
Trong số đó, TiS₂ là một hợp chất phân lớp và tương tác giữa các lớp là Lực Van der Waals (Lực Van der Waals). Các ion lithium nhỏ hơn có thể đi vào các lớp TiS₂ và trải qua quá trình truyền điện tích cũng như lưu trữ các ion lithium, tương tự như Khi ép mứt vào bánh sandwich, quá trình này là sự xen kẽ của các ion [4] [5]. Trong quá trình phóng điện, các ion Li+ trong chất điện phân được chèn vào giữa các lớp TiS₂ của điện cực dương, nhận điện tích và hình thành LixTiS₂.
Pin lithium thứ cấp ở giai đoạn này chủ yếu sử dụng lithium kim loại làm vật liệu điện cực âm, tuổi thọ và độ an toàn của pin được cải thiện bằng cách cải tiến vật liệu điện cực dương. Là loại pin lithium thứ cấp được thương mại hóa sớm nhất, lithium kim loại được sử dụng làm vật liệu điện cực âm có điện thế âm thấp. Pin có mật độ năng lượng cao và tương đối di động. Tuy nhiên, độ an toàn của nó cũng bị nghi ngờ rộng rãi. Vào cuối mùa xuân năm 1989, pin lithium kim loại thế hệ đầu tiên do công ty Moli Energy của Canada sản xuất phát nổ, điều này cũng khiến việc thương mại hóa pin lithium kim loại rơi vào bế tắc.
Để nâng cao tính an toàn của pin lithium, việc phát triển vật liệu điện cực mới là rất quan trọng đối với pin lithium. Tuy nhiên, việc sử dụng các hợp chất lithium khác làm điện cực âm thay vì lithium sẽ làm tăng thế điện cực âm, giảm mật độ năng lượng của pin lithium và giảm dung lượng pin. Vì vậy, việc tìm kiếm vật liệu điện cực mới phù hợp cũng trở thành bài toán khó trong lĩnh vực nghiên cứu pin lithium.
Khoảng năm 1980, John Bannister Goodenough và những người khác giảng dạy tại Đại học Oxford ở Vương quốc Anh đã phát hiện ra lithium coban oxit LiCoO₂ (LCO), một hợp chất có thể chứa các ion lithium. LiCoO₂ có tiềm năng cao hơn các vật liệu catốt khác vào thời điểm đó. Điều này cho phép pin lithium sử dụng LiCoO₂ làm điện cực dương để cung cấp điện áp cao hơn và dung lượng pin cao hơn.
Tinh thể oxit lithium coban có cấu trúc phân lớp và thuộc hệ tinh thể lục giác . Trong số đó, mạng bát diện gồm các nguyên tử O và Co được sắp xếp trên mặt phẳng thành các lớp CoO₂ và các lớp CoO₂ được ngăn cách với nhau bằng các ion lithium và tạo thành kênh truyền ion lithium phẳng. Điều này cho phép oxit lithium coban vận chuyển các ion lithium nhanh hơn thông qua kênh ion lithium phẳng. Quá trình tách và chèn các ion lithium trong oxit lithium coban tương tự như quá trình xen kẽ. Oxit lithium coban có thể duy trì sự ổn định của cấu trúc tinh thể của nó trong quá trình tích điện và phóng điện nhẹ. Tuy nhiên, với việc loại bỏ dần các ion lithium, oxit lithium coban có xu hướng biến đổi thành hệ tinh thể đơn tà [2]. Trong pin lithium sử dụng lithium coban oxit làm điện cực dương, trong quá trình phóng điện, phản ứng xảy ra ở điện cực dương là:
Điện cực dương: Li1-xCoO₂ + xLi+ + xe- → LiCoO₂
So với titan disulfua, vật liệu catốt lithium coban oxit có tiềm năng catốt cao hơn, đồng thời cấu trúc phân lớp của lithium coban oxit có thể vận chuyển các ion lithium nhanh hơn, khiến nó trở thành vật liệu catốt tuyệt vời cho pin lithium-ion.
Cùng năm đó, Rachid Yazami đã phát hiện ra hiện tượng xen kẽ ion tuần hoàn của các ion lithium trong than chì và xác minh tính khả thi của than chì làm cực âm cho pin lithium [10]. Than chì có cấu trúc dạng lớp và tương tự như TiS₂, các lớp trong than chì được kết nối bởi lực van der Waals yếu, cho phép các ion lithium nhỏ hơn đi vào các lớp than chì và gây ra sự truyền điện tích.

Trong bài báo năm 1983 của mình, Yazami đã sử dụng phương pháp điện phân trạng thái rắn polyethylene oxit-lithium perchlorate và sử dụng kim loại lithium làm điện cực âm và than chì làm điện cực dương để tạo thành pin sơ cấp. Trong quá trình phóng điện, than chì đóng vai trò là điện cực dương trải qua phản ứng sau:
nC + e- + Li+ → (nC, Li)
Khi đó xảy ra: (nC, Li) → LiCn
Trong quá trình phóng điện của pin ban đầu với than chì làm điện cực dương, các ion lithium trải qua phản ứng xen kẽ trong lớp than chì, xảy ra sự truyền điện tích và hợp chất LiCn được hình thành.
Sự xuất hiện của pin lithium-ion
Năm 1982, Yoshino Akira, người làm việc cho Tập đoàn Asahi Kasei ở Nhật Bản, đã chế tạo một mẫu pin lithium-ion sử dụng lithium coban oxit làm điện cực dương và polyacetylene (C2H2)n làm điện cực âm. Trong quá trình phóng điện của pin lithium coban oxit, các ion lithium di chuyển từ điện cực dương của pin sang oxit lithium coban thông qua chất điện phân để xả pin.Tuy nhiên, pin lithium coban oxit vẫn còn nhiều vấn đề. Điện cực âm của pin, polyacetylene, có mật độ năng lượng thấp và độ ổn định thấp. Do đó, Akira Yoshino đã sử dụng vật liệu giống than chì mới “carbon mềm” thay vì polyacetylene làm vật liệu điện cực âm của pin, và chuẩn bị nguyên mẫu pin lithium-ion đầu tiên vào năm 1985 và xin cấp bằng sáng chế [10]. Nguyên mẫu pin lithium-ion do Akira Yoshino thiết kế đã trở thành nền tảng cho nhiều loại pin hiện đại.
So với pin lithium, pin nguyên bản do Akira Yoshino thiết kế sử dụng vật liệu cacbon làm điện cực âm và oxit lithium coban làm điện cực dương để loại bỏ lithium kim loại, vì vậy loại pin này còn được gọi là "pin lithium-ion" . Bởi vì trong pin lithium-ion lithium coban oxit, các ion lithium trải qua các phản ứng xen kẽ ở cả điện cực dương và âm, và sự truyền điện tích nhanh chóng đạt được thông qua sự xen kẽ nhanh chóng của các ion lithium, nên cấu trúc pin này còn được gọi một cách sống động là pin ghế bập bênh.
Năm 2019, Giải Nobel Hóa học đã được trao cho nhà khoa học người Mỹ John B. Goodenough, nhà khoa học người Anh M. Stanley Whittingham và nhà khoa học Nhật Bản Yoshino Akira Yoshino, để ghi nhận những đóng góp nghiên cứu của họ đối với pin lithium-ion.

Sự xuất hiện của pin lithium-ion sử dụng vật liệu carbon làm điện cực âm và oxit lithium coban làm điện cực dương đã thúc đẩy sự phát triển của pin lithium-ion. Khi các nhà nghiên cứu dần dần nghiên cứu sâu hơn về pin lithium-ion, ba hệ thống đã được phát triển cho vật liệu cực âm của pin lithium-ion: lithium coban oxit (LCO), lithium sắt photphat (LFP) và mangan coban niken bậc ba (NMC/NCM). ) ). hệ thống. Trong số đó, hệ thống lithium coban oxit có dung lượng pin tương đối cao hơn và đóng vai trò quyết định trong lĩnh vực sản phẩm điện tử 3C như điện thoại di động và máy tính mà chúng ta thường sử dụng. Hệ thống lithium sắt photphat và hệ thống lithium bậc ba có độ ổn định cao hơn và được sử dụng rộng rãi trong các phương tiện năng lượng mới.
Sự xuất hiện của pin lithium-ion đã thay đổi hoàn toàn cách chúng ta sống. So với pin niken-cadmium và pin niken-hydrua kim loại, pin lithium-ion có mật độ năng lượng cao hơn, pin lithium-ion có cùng dung lượng pin sẽ dễ mang theo hơn và có thể hỗ trợ mức tiêu thụ điện năng cao cho điện thoại thông minh có nhiều chức năng phong phú. Đồng thời, hầu hết pin lithium-ion không có hiệu ứng nhớ và không cần phải xả hết trước khi sạc lại, do đó, pin lithium-ion có thể được sạc theo yêu cầu. So với pin lithium, tốc độ sạc của pin lithium-ion được cải thiện đáng kể. Và tốc độ sạc nhanh của pin lithium-ion hỗ trợ rất nhiều cho cuộc sống của chúng ta. Do đó, trong các tình huống ứng dụng như điện thoại di động, máy tính di động và phương tiện sử dụng năng lượng mới, pin lithium-ion đã dần thay thế pin niken-cadmium và pin hydrua kim loại niken trong một số tình huống nhờ hiệu suất tuyệt vời của chúng.
Tuổi thọ pin điện thoại di động ngắn hơn khi sử dụng nhiều hơn không?
Nỗi đau của pin niken-cadmium - hiệu ứng trí nhớĐối với pin niken-cadmium, các hạt tinh thể cadmium ở điện cực âm của pin niken-cadmium được chuẩn bị thiêu kết tương đối thô, khi pin niken-cadmium không được sạc đầy và xả trong thời gian dài, các hạt tinh thể cadmium dễ bị đến sự tập hợp và kết tụ. Tại thời điểm này, nền xả thứ cấp được hình thành khi pin xả. Pin sẽ sử dụng nền xả thứ cấp này làm điểm cuối của quá trình xả pin, dung lượng pin sẽ thấp và pin sẽ chỉ ghi nhớ dung lượng thấp này trong quá trình xả tiếp theo. Đây là lý do tại sao điện thoại di động thế hệ cũ sử dụng pin niken-cadmium thường được khuyến nghị xả hết pin trước khi sạc. Tuy nhiên, với sự cải tiến liên tục của công nghệ xử lý pin niken-cadmium và pin hydrua kim loại niken, tác động của hiệu ứng bộ nhớ đến dung lượng pin liên tục giảm và tác hại của việc sạc đầy và xả đối với tuổi thọ pin dần trở nên rõ ràng.

Sạc và xả pin lithium-ion quá mức dẫn đến giảm tuổi thọ
Lithium coban oxit có công suất lý thuyết cao, nhưng công suất thực tế của lithium coban oxit khác xa so với công suất lý thuyết trong quá trình sử dụng. Bởi vì sau khi chúng ta sạc và xả pin lithium-ion vượt quá dung lượng này, lithium coban oxit sẽ trải qua quá trình sạc và xả không thể đảo ngược mà chúng ta thường gọi là sạc quá mức hoặc xả quá mức cho pin. Quá trình này đi kèm với sự thay đổi pha cấu trúc của oxit lithium coban, làm giảm dung lượng của pin.
Khi pin bị sạc quá mức, một lượng lớn ion lithium được giải phóng khỏi điện cực âm của oxit lithium coban và các ion lithium còn lại không đủ để hỗ trợ cấu trúc ban đầu của oxit lithium coban, khiến tinh thể Li1-xCoO₂ thay đổi từ từ hệ tinh thể lục giác sang hệ đơn tà, cấu trúc lục giác ban đầu bị sụp đổ do thiếu sự hỗ trợ của ion. Trong quá trình này, sự biến đổi pha của oxit lithium coban không thể đảo ngược hoàn toàn, các thông số tế bào đơn vị của oxit lithium coban thay đổi, ứng suất thay đổi và các chỗ trống lithium ion bị nén, khiến dung lượng của pin lithium-ion bị suy giảm.
Tính không ổn định của pin lithium-ion điện áp cao
Ngoài sự thay đổi không thể đảo ngược về dung lượng pin do sự thay đổi pha cấu trúc của oxit lithium coban, việc tăng điện áp đầu ra của pin lithium-ion còn khiến các phản ứng phụ khác dễ xảy ra ở pin lithium-ion và tuổi thọ của lithium -ion pin bị giảm. Hiện nay, điện thoại thông minh trên thị trường thường sử dụng điện áp sạc và xả khoảng 4,4V. Điện áp cao có thể làm tăng dung lượng của pin lithium-ion và tăng tốc độ sạc và xả của pin lithium-ion. Nhưng điều tiếp theo là sự gia tăng các phản ứng phụ trên bề mặt điện cực của pin lithium-ion và một loạt tác dụng phụ như sự mất ổn định của chất điện phân ở điện áp cao.

Chất điện phân của pin lithium-ion phản ứng ở giao diện rắn-lỏng với các điện cực dương và âm để tạo thành lớp thụ động bao phủ bề mặt điện cực. Lớp thụ động này có đặc tính của chất điện phân rắn, các ion Li có thể được đưa vào và tách ra một cách tự do thông qua lớp thụ động, do đó, màng thụ động này được gọi là “màng giao diện chất điện phân rắn” (gọi tắt là màng SEI). Quá trình hình thành màng SEI sẽ tiêu thụ một số ion lithium, gây ra tình trạng mất dung lượng pin lithium-ion không thể khắc phục được. Dưới tác động của điện áp cao, các phản ứng phụ trên bề mặt các điện cực này diễn ra nghiêm trọng khiến dung lượng pin giảm dần.
Những điều cần chú ý khi sử dụng điện thoại di động
Không sạc ở nhiệt độ caoKhông sạc điện thoại khi nó quá nóng hoặc quá lạnh. Khi điện thoại di động quá nóng, việc sạc pin lithium-ion trong điều kiện nhiệt độ cao cũng sẽ thay đổi cấu trúc điện cực dương và âm của pin lithium-ion, dẫn đến dung lượng pin bị suy giảm không thể khắc phục. Do đó, hãy cố gắng tránh sạc điện thoại trong điều kiện quá lạnh hoặc quá nóng, điều này cũng có thể kéo dài tuổi thọ sử dụng của điện thoại một cách hiệu quả.

Trong quá trình sử dụng các sản phẩm kỹ thuật số như điện thoại di động, máy tính xách tay hoặc máy tính bảng, nếu phát hiện nắp lưng pin bị biến dạng, pin bị phồng hoặc các tình trạng bất thường khác thì chúng ta phải ngừng sử dụng kịp thời và thay pin cho nhà sản xuất, và cố gắng tránh các vấn đề do sử dụng pin gây ra.









