Mẫn Nhi
Admin xinh gái
Một lô thuốc nhỏ mắt Natri clorid 0,9% quen thuộc vừa chính thức bị Cục Quản lý Dược (Bộ Y tế) yêu cầu thu hồi trên phạm vi toàn quốc. Đây là loại thuốc thường có mặt trong tủ thuốc của nhiều gia đình, nhưng kết quả kiểm nghiệm mới nhất cho thấy sản phẩm không đảm bảo các tiêu chuẩn chất lượng cần thiết để lưu hành an toàn trên thị trường. Việc thu hồi này nhằm ngăn chặn các rủi ro tiềm ẩn cho người sử dụng khi dùng phải sản phẩm không đạt chuẩn.
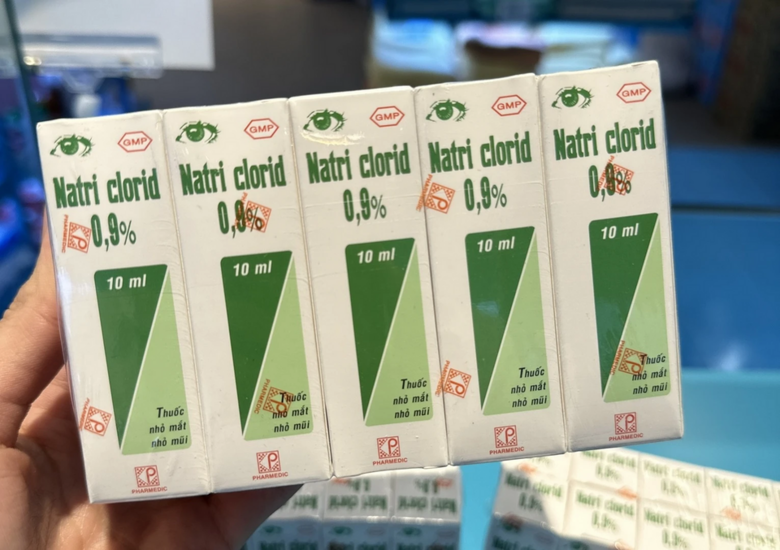
Thuốc nhỏ mắt Natri clorid 0,9% do Công ty cổ phần Dược phẩm Dược liệu Pharmedic sản xuất.
Cụ thể, mẫu thuốc kiểm nghiệm đã không đạt tiêu chuẩn về chỉ tiêu "độ trong" – một yêu cầu kỹ thuật bắt buộc đối với các loại thuốc dùng cho mắt để đảm bảo không gây kích ứng hay tổn thương cho người dùng. Lô thuốc vi phạm có số giấy đăng ký lưu hành 893100060724, số lô 10370725, được sản xuất vào ngày 14/7/2025 và có hạn dùng đến ngày 14/1/2028.
Để đảm bảo tính khách quan và chính xác, Viện Kiểm nghiệm thuốc TP.HCM đã tiếp tục lấy mẫu bổ sung. Kết quả tại phiếu kiểm nghiệm số 0436/VKN-YC2026 ngày 29/4/2026 một lần nữa khẳng định lô thuốc trên tiếp tục không đạt tiêu chuẩn về độ trong. Dựa trên những bằng chứng cụ thể này, Cục Quản lý Dược đã quyết định thực hiện lệnh thu hồi trên toàn quốc.
Pharmedic cũng là đơn vị chịu mọi chi phí liên quan đến việc thu hồi, xử lý thuốc vi phạm cũng như bồi thường thiệt hại theo luật định. Sau khi hoàn tất, báo cáo kết quả phải được gửi về Cục Quản lý Dược cùng Sở Y tế các tỉnh Quảng Ngãi và TP.HCM trong vòng 3 ngày.
Sở Y tế các địa phương cũng được giao nhiệm vụ công bố rộng rãi thông tin này trên các cổng thông tin điện tử, tăng cường thanh tra và giám sát để đảm bảo không còn sản phẩm lỗi nào lưu thông trên thị trường, xử lý nghiêm các trường hợp không chấp hành lệnh thu hồi.

Thuốc nhỏ mắt Natri clorid 0,9% do Công ty cổ phần Dược phẩm Dược liệu Pharmedic sản xuất.
Vấn đề về độ trong của lô thuốc nhỏ mắt Pharmedic
Lô thuốc bị thu hồi là Dung dịch nhỏ mắt Natri clorid 0,9%, do Công ty cổ phần Dược phẩm Dược liệu Pharmedic sản xuất. Theo quyết định do Phó Cục trưởng Cục Quản lý Dược Tạ Mạnh Hùng ký ban hành, sản phẩm này bị xác định vi phạm chất lượng mức độ 3.Cụ thể, mẫu thuốc kiểm nghiệm đã không đạt tiêu chuẩn về chỉ tiêu "độ trong" – một yêu cầu kỹ thuật bắt buộc đối với các loại thuốc dùng cho mắt để đảm bảo không gây kích ứng hay tổn thương cho người dùng. Lô thuốc vi phạm có số giấy đăng ký lưu hành 893100060724, số lô 10370725, được sản xuất vào ngày 14/7/2025 và có hạn dùng đến ngày 14/1/2028.
Kết quả kiểm nghiệm từ các cơ quan chức năng
Sự việc bắt đầu khi Trung tâm Kiểm nghiệm thuốc, mỹ phẩm, thực phẩm tỉnh Quảng Ngãi tiến hành lấy mẫu kiểm tra tại Quầy thuốc Kim Liên (thôn An Hội Nam 1, xã Trà Giang, tỉnh Quảng Ngãi). Phiếu kiểm nghiệm số 221/PKN ngày 30/1/2026 tại đây đã bước đầu xác định mẫu thuốc không đạt chất lượng.Để đảm bảo tính khách quan và chính xác, Viện Kiểm nghiệm thuốc TP.HCM đã tiếp tục lấy mẫu bổ sung. Kết quả tại phiếu kiểm nghiệm số 0436/VKN-YC2026 ngày 29/4/2026 một lần nữa khẳng định lô thuốc trên tiếp tục không đạt tiêu chuẩn về độ trong. Dựa trên những bằng chứng cụ thể này, Cục Quản lý Dược đã quyết định thực hiện lệnh thu hồi trên toàn quốc.
Trách nhiệm của doanh nghiệp và hệ thống phân phối
Sau khi có lệnh thu hồi, Công ty Pharmedic phải ngay lập tức dừng việc kinh doanh và thực hiện biệt trữ toàn bộ số thuốc còn tồn kho. Trong vòng 7 ngày, doanh nghiệp cần báo cáo chi tiết tình hình phân phối lô thuốc này tới các cơ sở bán buôn và khám chữa bệnh. Thời hạn để hoàn tất việc thu hồi toàn bộ lô thuốc trên thị trường là 30 ngày.Pharmedic cũng là đơn vị chịu mọi chi phí liên quan đến việc thu hồi, xử lý thuốc vi phạm cũng như bồi thường thiệt hại theo luật định. Sau khi hoàn tất, báo cáo kết quả phải được gửi về Cục Quản lý Dược cùng Sở Y tế các tỉnh Quảng Ngãi và TP.HCM trong vòng 3 ngày.
Sự phối hợp của các cơ sở y tế và cơ quan quản lý
Cục Quản lý Dược đã yêu cầu tất cả các cơ sở bán buôn, bán lẻ và chuỗi nhà thuốc ngừng ngay việc cung cấp và cấp phát lô thuốc vi phạm này, đồng thời tổ chức trả lại hàng cho đơn vị cung ứng. Đối với các bệnh viện và cơ sở khám chữa bệnh, các bác sĩ cần ngừng kê đơn và thông báo cho bệnh nhân.Sở Y tế các địa phương cũng được giao nhiệm vụ công bố rộng rãi thông tin này trên các cổng thông tin điện tử, tăng cường thanh tra và giám sát để đảm bảo không còn sản phẩm lỗi nào lưu thông trên thị trường, xử lý nghiêm các trường hợp không chấp hành lệnh thu hồi.